ポイント
- サウジアラビアの皮膚科医が、韓国製のエクソソーム注射による皮膚壊死を報告。
- ニキビ治療のために注射をしたところ、傷跡が残り、色素の沈着が残った。
- 製品は未承認で、メーカーは注射でなく塗布やマイクロニードル使用を推奨していた。
注射。写真はイメージ。(写真/Adobe Stock)
エクソソーム製剤を用いた美容医療において、重い合併症が報告された。
サウジアラビアの皮膚科医が2025年8月に美容皮膚科専門誌「Journal of Cosmetic Dermatology」で報告したもので、韓国製の未承認エクソソーム製剤を塗るための製品ではあったが、顔面に注射された男性が虚血性壊死(皮膚壊死の一種で、血流が滞って組織が死んだ状態になること)を起こす事態となった。
塗るためと推奨される製剤を注射
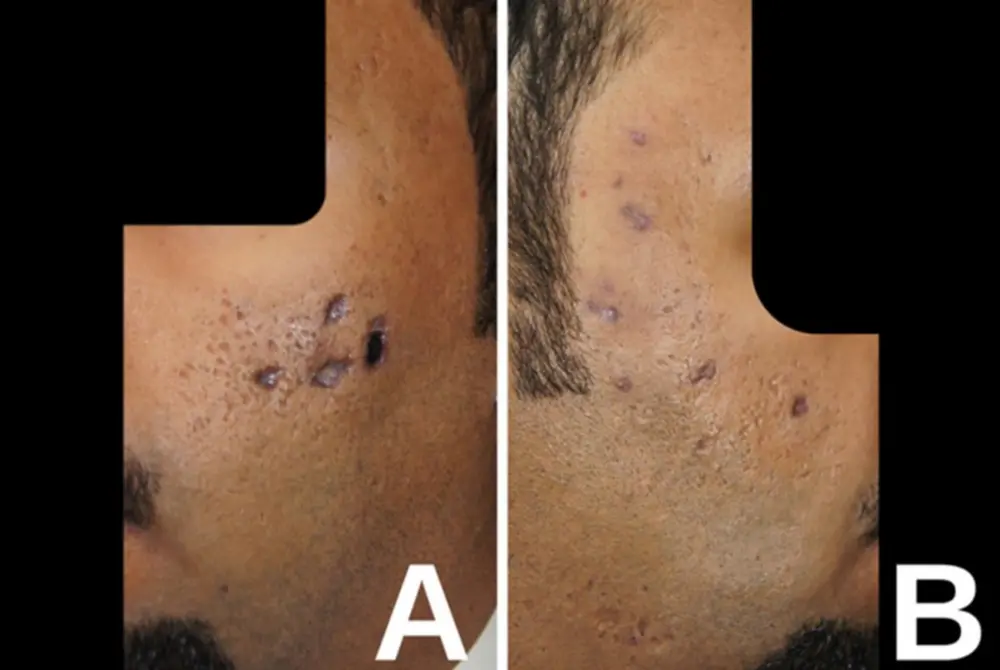
両頬に壊死や色素の沈着が起きた。Aは左の顔面、Bは右の顔面。(出典/J Cosmet Dermatol
. 2025;24:e70387. )
- 事例の概要→38歳男性がニキビ跡治療目的で、皮膚科医ではない医師により韓国製未承認エクソソーム製剤を顔に注射された。
- 施術内容→製品はヒト臍帯血由来成分を含む凍結乾燥製剤。本来は塗布やマイクロニードル使用が推奨されていたが、皮膚内に直接注射された。
- 副作用の発症→施術3日後、頬に紫色の変色と潰瘍性皮膚変化が出現し、強い痛みを伴った。血流障害による部分的壊死と判断。
報告によれば、注射を行ったのは皮膚科医ではない報告者とは別の医師であり、報告者はその後診察を行った皮膚科医となる。
問題は38歳男性に起こった。皮膚科医ではない医師が、ニキビ跡の治療目的で、韓国製の凍結乾燥エクソソーム製剤を顔面に注射。使用された製品は、韓国製の未承認エクソソーム製剤で、ヒト臍帯血由来の培養液成分を含んでいた。メーカーは注射でなく塗布やマイクロニードル使用を推奨していたが、実際には皮膚内に注射されたとされている。
施術から3日後、頬に紫色の変色を伴う潰瘍性の皮膚の変化が出現。強い痛みが起こり、血液検査などでは感染していることは確認できず、血流が滞ったことによる部分的な壊死と判断された。
結果として、萎縮性瘢痕と色素沈着が残る結果になった。報告者は後にレーザー治療を行ったが改善は限定的だった。
※萎縮性瘢痕とは、皮膚が縮むような形で傷跡が残るもの。
製品によって小さな血管の詰まり、血管の圧迫などの可能性が考えられたが、皮膚を採取した検査は同意を得られなかった。
従来、美容医療での皮膚の壊死は、ヒアルロン酸などの注入によって報告されている。
ヒアルロン酸の場合には、ヒアルロニダーゼの使用によって回復が可能だが、エクソソームではそうはいかない。報告によれば、今回のケースでは、壊死は血管障害によるものと考えられ、既に進行していたため、ヒアルロン酸注入に用いられるような分解酵素(ヒアルロニダーゼ)による救済処置は不可能であった。
論文によれば、過去に36歳男性の類似した症例が報告されていた。このケースでは壊死の跡と色素の沈着が残っていたと説明している。ただし、過去症例では一部改善も報告していた。
報告者は、未承認の製品の使用に伴うリスクを強調している。
厚労省も「細胞加工物と同等のリスク」

厚生労働省。(写真/Adobe Stock)
- 自由診療で拡大→エクソソームや幹細胞培養上清を用いた治療が、美容医療を中心に広がっている。
- 法規制の対象外→細胞を含まないため「安確法」の対象外とされてきたが、リスクが指摘されている。
- 今後の動向→再生医療の提供計画に安全性評価項目を追加するなど、制度整備が進む可能性が高い。
日本国内でも、エクソソームを含む細胞外小胞(EVs)や幹細胞培養上清を用いた治療法については、近年、美容医療の領域を中心に自由診療としての実施が拡大している。
これらは細胞を含まないことを理由に、現行法では「再生医療等の安全性の確保等に関する法律(安確法)」の対象外とされてきた。
こうした中、2024年12月16日に開催された厚生科学審議会再生医療等評価部会において、EVsや培養上清に対する中間報告が公表された。同報告では、それらが既存の「細胞加工物」と同等のリスクを有する可能性があると指摘され、法的規制の必要性や、品質・製造工程の厳格な管理体制の整備が求められるとの見解が示された。
とりわけ、「エクソソーム療法」については、安全性を裏付ける科学的根拠が乏しい点が問題視されており、品質管理の不備や不透明な提供実態が、健康被害につながるおそれがあるとの懸念が強まっている。
自由診療下では、過去に敗血症等の重篤な副作用も報告され、今後、再生医療の提供計画や報告書類への安全性評価項目の追加など、制度的整備が進む可能性が高い。
安全性の裏付けがない製剤を、想定を超えた方法で使用することは危険を伴うことを理解することが重要だろう。
参考文献
AlBargawi S. Necrosis Following Dermal Injection of Lyophilized Exosomes: A Case Report. J Cosmet Dermatol. 2025 Aug;24(8):e70387. doi: 10.1111/jocd.70387. PMID: 40820962; PMCID: PMC12359287.
https://pubmed.ncbi.nlm.nih.gov/40820962/
国際幹細胞学会が自由診療の再生医療などに改善を要求、エクソソーム、点滴治療、PRPなどどうなる?増える再生医療クリニックでは淘汰が進む可能性も
https://biyouhifuko.com/news/world/11617/
iPS細胞由来エクソソーム治療に注意喚起、「科学的根拠が不足している」、日本再生医療学会が声明を発表
https://biyouhifuko.com/news/japan/10627/
培養上清やエクソソーム、無視できないリスクの存在、規制強化の可能性、EVs(細胞外小胞)の議論を求める意見、厚生労働省の中間報告で示された課題と展望
https://biyouhifuko.com/news/japan/10434/








